پرتوزایی
پَرتوزایی (radioactivity)
(یا: رادیواکتیویته) تغییر خودبهخود هستهها[۱]ی اتم، همراه با گسیل تابش[۲]. چنین اتمهایی را پرتوزا[۳] مینامند. این خاصیت در ایزوتوپهای پرتوزای عناصر پایدار، و همۀ ایزوتوپهای عناصر پرتوزا مشاهده میشود. پرتوزایی ممکن است طبیعی باشد یا بهصورت القایی و مصنوعی پدید آید. هر مادۀ پرتوزا براثر آزادسازی تابش واپاشیده میشود و بهصورت مادۀ جدیدی درمیآید. تابش آزادشده در واپاشی بهصورت ذرات آلفا[۴] و ذرات بتا[۵] یا بهصورت امواج الکترومغناطیسی[۶] پرانرژی با نام تابش گاما[۷] است. عناصر پرتوزای طبیعی عناصری با عدد اتمی[۸] ۸۳ یا بیشترند. عناصر پرتوزا را بهصورت مصنوعی نیز تولید میکنند. پرتوزایی با وسایلی مثل لامپ گایگر ـ مولر[۹]، صفحات عکاسی، یا الکتروسکوپ (برقنما)[۱۰] آشکارسازی میشود. شمارشگر الکترونیکی[۱۱] متصل به سنجشافزار گایگر ـ مولر مقدار تابش آشکارسازیشده را بهصورت رقمی نمایش میدهد.
کشف پرتوزایی. برای نخستینبار، پرتوزایی را فیزیکدان فرانسوی، هانری بکرل[۱۲]، در ۱۸۹۶ هنگامی کشف کرد که صفحات عکاسیاش، که روکشهای حفاظتی کاملی داشتند، در مجاورت بعضی ترکیبات اورانیوم[۱۳] سیاه و لکهدار شدند. بررسی دقیقتر نشان داد که روکشهای فلزی نازک نمیتوانند از سیاهشدگی صفحات عکاسی جلوگیری کنند. بهروشنی معلوم شد از ترکیبات اورانیوم تابشی گسیل میشود که از روکش فلزی نیز میگذرد. طولی نکشید که پیِر و ماری کوری[۱۴] موفق به جداسازی عناصر پرتوزای دیگری شدند. یکی از این عناصر رادیوم[۱۵] بود که پرتوزایی آن بیش از ۱میلیون برابر پرتوزایی اورانیوم است.
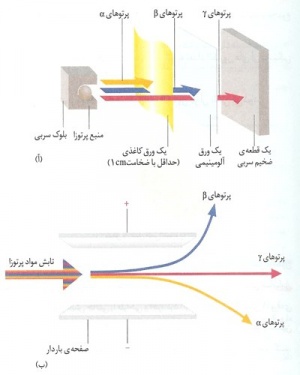
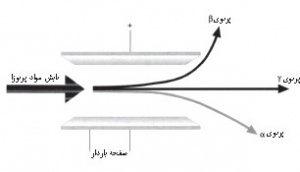
تابشهای گسیلشده در پرتوزایی. درپی تحقیقات بیشتر ارنست رادرفورد[۱۶] برای پیبردن به ماهیت تابش، معلوم شد که سه نوع تابش در پرتوزایی گسیل میشود: ذرات آلفا، ذرات بتا، و پرتوهای گاما. ذرات آلفا ذراتی پرانرژی با بار مثبتاند که از هستههای اتمهای پرتوزا گسیل و از دو پروتون[۱۷] و دو نوترون[۱۸] تشکیل میشوند. درنتیجه، مانند هستۀ[۱۹] اتم هلیوم[۲۰]اند. در هوا، این ذرات بهعلت جرم زیادشان، برد کوتاهی در حد چند سانتیمتر دارند و حتی یک برگ کاغذ از حرکتشان جلوگیری میکند. ذرات بتا قدرت نفوذ بیشتری دارند و میتوانند به اندازۀ سه میلیمتر در آلومینیوم[۲۱] و حداکثر یک متر در هوا نفوذ کنند و به حرکتشان ادامه دهند. این ذرات از الکترونهایی پُرانرژی تشکیل میشوند که با سرعت زیاد از اتمهای پرتوزایی گسیل میشوند که خودبهخود فرو میپاشند. پرتوهای گاما چیزی جز تابش الکترومغناطیسی بسیار پُرانرژی نیستند. پرتوهای گاما بسیار پرنفوذند و فقط در برخورد مستقیم با اتمها متوقف میشوند. بُرد نفوذ این پرتوها در سرب به حدود چهار سانتیمتر میرسد. تابشهای آلفا، بتا، و گاما ضمن گذار از محیطهای مادی، معمولاً با الکترونهای اتمی برخورد میکنند که موجب کَندهشدن الکترون و یونیدگی[۲۲] اتمها میشود. بههمینسبب، چنین تابشهایی را تابش یوننده[۲۳] مینامند. ذرات آلفا، با توجه به سنگینی و حرکت کُند و حمل دو بارِ مثبت، از بیشترین خاصیت یونندگی برخوردارند. پرتوهای گاما بهعلت بیباربودن یونندگی ضعیفی دارند. ذرات بتا از لحاظ توان یونندگی بین تابشهای آلفا و گاما قرار میگیرند.
آشکارسازی پرتوزایی. در آشکارسازهای تابشهای یوننده، از خواص یونندگی تابش برای ایجاد تغییرات قابل آشکارسازی و اندازهگیری استفاده میکنند. در شمارشگر گایگر[۲۴]، از جریان موقت در حال گذر بین الکترودها[۲۵] استفاده میکنند که هنگام عبور تابش یوننده از گاز مناسبِ درون آشکارساز ایجاد میشود. این وسیله را به افتخار فیزیکدان آلمانی، هانس گایگر[۲۶]، نامگذاری کردهاند. مقدار فعالیت هر منبع پرتوزا[۲۷] را با یک فروپاشی هستههای در آن مشخص میکنند. بنابه تعریف، یک فروپاشی در هر ثانیه را، یک بکرل Bq میگویند.
واپاشی پرتوزا. هرگاه هستهای ناپایدار از خود تابش آلفا، بتا یا گاما گسیل کند تا به وضعیت پایدارتر برسد، واپاشی پرتوزا صورت میگیرد. تابش گسیلشده از اتمهای فروپاشنده را تابش اتمی[۲۸] میگویند. هر ذرۀ آلفا از دو پروتون و دو نوترون تشکیل میشود. وقوع واپاشی آلفازا یا گسیل ذرۀ آلفا از هسته به شکلگیری هستهای جدید منجر میشود. اتمهای ایزوتوپ اورانیوم با جرم ۲۳۸ براثر گسیل یک ذرۀ آلفا به اتم توریوم با جرم ۲۳۴ تبدیل میشوند. در واپاشی بتازا، که بهصورت گسیل الکترون از هستۀ اتمی تحقق مییابد، یک نوترون به یک پروتون تبدیل میشود و عدد اتمی به اندازۀ یک واحد افزایش مییابد. مثلاً واپاشی بتازای ایزوتوپ کربن[۲۹] چهارده منجر به تشکیل یک اتم نیتروژن با جرم چهارده و عدد اتمی هفت، و گسیل یک الکترون میشود. گسیل گاما معمولاً همراه با واپاشیهای آلفازا و بتازا صورت میگیرد. هنگام خروج ذرۀ آلفا یا بتا از هسته تابش الکترومغناطیسی[۳۰] پُرانرژی نیز از آن گسیل میشود و هستۀ باقیمانده به حالت پایدارتر میرسد. ایزوتوپهای گوناگون هر عنصر جرمهای اتمی[۳۱] متفاوت دارند. تعداد پروتونهای هستۀ ایزوتوپهای گوناگون در هر عنصر یکسان، ولی شمار نوترونهای آنها متفاوت است. مثلاً، ایزوتوپهای اورانیومِ ۲۳۵ و اورانیومِ ۲۳۸، هر دو ۹۲ پروتون دارند، ولی تعداد نوترونها در اولی ۱۴۳ و در دومی ۱۴۶ است. بعضی از ایزوتوپها پرتوزای طبیعیاند. واپاشی پرتوزا ممکن است طی یک مرحله یا مراحلی صورت گیرد که به واپاشی سِری یا زنجیری معروف است. گاهی پرتوزایی بعضی از عناصر محصول نسبت به عنصر مادر بیشتر است.
آهنگ واپاشی پرتوزا. گسیل پرتوزایی اتمها خودبهخود و کاملاً پیشبینیناپذیر است، اما در نمونهای شامل تعداد بسیار بسیار زیاد اتم پرتوزا، بهنظر میرسد آهنگ کلی واپاشی را شمار هستههای ناواپاشیدۀ باقیمانده تعیین میکند. زمان لازم برای واپاشیدهشدن نیمی از اتمهای پرتوزای هر نمونه مقدار ثابتی است که آن را نیمعمر[۳۲] مینامند. مواد پرتوزا در طول زمان بهصورت نمایی واپاشیده میشوند و مقدار نیمعمر آنها نیز ممکن است بین کسری از ثانیه تا میلیاردها سال متفاوت باشد.
مخاطرات زیستی. زندگی انسان و محیط او با مواد پرتوزا درآمیخته است. غذای انسان دارای مقادیر ناچیزی از ایزوتوپهای پرتوزاست و بدن نیز شامل موادی است که بعضاً بهطور طبیعی پرتوزایند. بهعلاوه، انسان همواره تحت تابش ذرات باردار پرانرژیای قرار دارد که از فضای خارج سرچشمه میگیرند. تابش محیط را تابش زمینه[۳۳] میگویند که هنگام بررسی مخاطرات پرتوگیری از سایر منابع بهحساب میآید. تابشهای آلفا، بتا، و گاما را بهسبب خواص یونسازی آنها، بهویژه هنگامی که جسم پرتوزا از راه غذا یا تنفس وارد بدن میشود، خطرناک میدانند. بیماری ناشی از پرتوگیری به شکلهای گوناگون ظاهر میشود و به بیماری تابشی[۳۴] معروف است.
کاربرد پرتوزایی. کاربرد پرتوزایی در علوم نوین نیازمند دقت، هدایت، و نظارت است. برای پیگیری مسیر حرکت واکنشهای شیمیایی یا فرایندهای فیزیکی و زیستشناختی از مقادیر جزئی عناصر پرتوزا بهمنزلۀ ردیاب استفاده میکنند. عمرسنجی پرتوکربنی[۳۵] روشی برای اندازهگیری سن مواد آلی است. تعیین سن سنگها نیز با پرتوزایی صورت میگیرد. گسیلهای پرتوزا و تابش الکترومغناطیسی را در پزشکی برای درمان نیز بهکار میبرند که درمان بعضی از سرطانها با استفاده از دُز تابشی دقیقاً کنترلشده از آن جمله است.
شکافت و گداخت هستهای. وقتی هستهای به دو پارۀ تقریباً مساوی تقسیم میشود، شکافت هستهای[۳۶] اتفاق میافتد. شکافت هسته منجر به آزادسازی تعدادی نوترون و مقدار فراوانی انرژی میشود. در راکتور هستهای[۳۷]، براثر بمباران هستههای اورانیوم ۲۳۵ با نوترون تولید شکافت میکنند. هنگامی که نوترونهای حاصل از شکافت هستهای اتمی، به شکافت هستههای دیگر ادامه دهند، واکنش زنجیری[۳۸] هستهای صورت میگیرد. این فرآیند را در راکتورهای هستهای بهدقت کنترل، و از انرژی هستهای[۳۹] آزادشده استفاده میکنند. در گداخت هستهاي[۴۰]، با ادغام دو هستۀ سبک هستهای بزرگتر تولید میکنند. گُداخت با آزادسازی مقادیر فراوان انرژی همراه است و در آینده منبع تولید انرژی تجاری خواهد بود. با این همه، بشر تاکنون به واکنش گُداخت قابل اتکایی دست نیافته است. کارکنان پژوهشگاه هستهای هاروِل در انگلستان برای جابهجایی مواد پرتوزا و اجرای عملیاتشان از اهرمها و دستهای مکانیکی استفاده میکنند. از این کارکنان با دیوارههایی از بتون و فولاد محافظت میکنند که ضخامتی بیش از یک متر دارند. پنجرهها از جنس شیشۀ دارای سرباند. در پایان هر روز کاری، کارکنان پس از آلودگیزدایی بسیار دقیق مرخص میشوند.
- ↑ nuclei
- ↑ emission of radiation
- ↑ radioactive
- ↑ alpha particles
- ↑ beta particles
- ↑ electromagnetic waves
- ↑ gamma radiation
- ↑ atomic number
- ↑ Geiger-Muller tube
- ↑ electroscope
- ↑ electronic counter
- ↑ Henri Becquerel
- ↑ Uranium
- ↑ Pierre and Marie Curie
- ↑ radium
- ↑ Ernest Rutherford
- ↑ protons
- ↑ neutrons
- ↑ nucleus
- ↑ helium
- ↑ aluminium
- ↑ ionizing
- ↑ ionizing radiation
- ↑ Geiger counter
- ↑ electrodes
- ↑ Hans Geiger
- ↑ radioactive source
- ↑ atomic radiation
- ↑ carbon
- ↑ electromagnetic radiation
- ↑ atomic mass
- ↑ half life
- ↑ background radiation
- ↑ radiation sickness
- ↑ radiocarbon dating
- ↑ nuclear fission
- ↑ nuclear reactor
- ↑ chain reaction
- ↑ nuclear energy
- ↑ nuclear fusion
