جدول تناوبی عناصر
جدول تناوبی عناصر (periodic table of the elements)

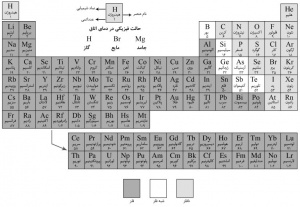
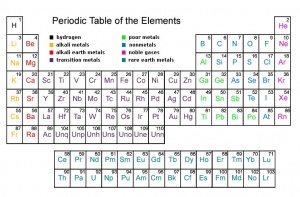

در شیمی، جدول ترتیبی عناصر براساس عدد اتمی[۱] آنها. این جدول براساس خواص عمدۀ عناصر شکل گرفته است و امکان پیشگویی رفتار آنها را فراهم میکند. در هر گروه، تشابه بسیار بین خواص عناصر بهچشم میخورد. ستونهای عمومی یا گروهها از اعداد یک تا هفت و نیز صفر شمارهگذاری شدهاند. این اعداد تعداد الکترونها را در خارجیترین لایۀ پرنشده و درنتیجه، ظرفیت[۲] ماکسیمم را نشان میدهد. واکنش پذیری[۳] یا فعالیت در هر گروه از بالا به پایین افزایش مییابد. نوعی روند خواص نیز ممکن است در ردیفهای افقی دیده شود که آن را دوره یا تناوب[۴] مینامند. خاصیت فلزی[۵] در یک تناوب از راست به چپ، و در یک گروه از بالا به پایین افزایش مییابد. بخش بزرگی از عناصر بین گروههای ۲ و ۳ متعلق به عناصر واسطهاند که یکی از ویژگیهای آنها دارا بودن بیش از یک حالت ظرفیتی است. این خصوصیات بهعلت ساختار هستهای و الکترونی اتمهای این عناصر ایجاد شده است. ارتباط بین موقعیتهای عناصر در جدول تناوبی و خواص عمدۀ آنها دانشمندان را قادر ساخته است که خواص عناصر دیگری مانند تکنیسیُم[۶] را پیشگویی کنند. عدد اتمی این عنصر ۴۳ است و اولینبار در ۱۹۳۷ سنتز شد. آرایش کنونی جدول تناوبی را، که براساس اعداد اتمی است، فیزیکدان انگلیسی، هنری موزلی[۷] طراحی کرد (۱۹۱۳ـ۱۹۱۴). جدول اصلی را، که براساس وزن اتمی[۸] طراحی شده بود، اولینبار شیمیدان انگلیسی، جان نیولندز[۹]، پیشنهاد (۱۸۶۳). در ۱۸۶۹، شیمیدان روس، دیمیتری مِندِلیِف[۱۰]، و شیمیدانی آلمانی با نام لوتار مایر[۱۱] این طرح را گسترش دادند.
